
blog
Sé que estos artículos pueden parecer similares entre sí. Todos hablan de procesos internos, de biología celular, de mecanismos que no se ven.
Pero hay una razón para eso.
La idea detrás de este blog no es venderte nada, es enseñarte cómo funciona tu cuerpo. Porque cuando entiendes qué factores aceleran el envejecimiento celular, puedes tomar decisiones más informadas. Pequeños cambios de hábitos que con el tiempo frenan ese proceso o al menos le dan a tu piel las condiciones para responder mejor.
Cada artículo es una pieza del mismo sistema. Mitocondrias, inflamación, hormonas, ejercicio, sueño, células zombi, todo está conectado. Y cuando lo ves completo, algo cambia en cómo te cuidas.
Cuarenta y cinco años en el calendario. Treinta y ocho en las células
O cincuenta y cinco.
Esa diferencia existe. Es medible. Y tiene un nombre: telómeros.
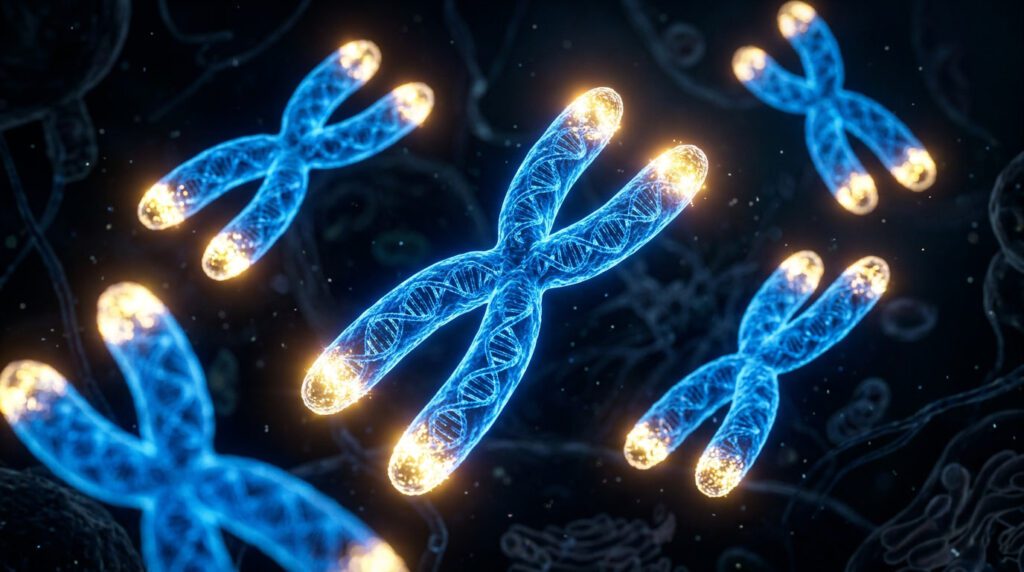
Imagina los cordones de tus zapatos. En los extremos tienen esas puntas plásticas pequeñas que evitan que el cordón se deshilache. Sin ellas el cordón se destruye con el uso.
Los telómeros hacen exactamente eso pero con tus cromosomas. Son secuencias de ADN que protegen los extremos de cada cromosoma para que no se deterioren ni se fusionen con otros.
Cuántos telómeros tienes — y cuánto se gastan
Cada célula humana tiene 46 cromosomas, y cada cromosoma tiene dos extremos. Eso significa que en cada célula de tu cuerpo hay 92 telómeros trabajando simultáneamente para proteger tu material genético.
Tu cuerpo tiene aproximadamente 37 billones de células. Casi todas con sus 92 telómeros intactos o en proceso de acortarse.
Cada vez que una célula se divide pierde entre 50 y 200 pares de bases de sus telómeros. Y una célula solo puede dividirse aproximadamente 40 a 60 veces a lo largo de su vida, lo que los científicos llaman el límite de Hayflick antes de que sus telómeros lleguen a un largo crítico y la célula entre en senescencia.
Es un proceso natural e inevitable. Pero la velocidad a la que ocurre — eso sí depende en gran parte de ti.
Cuando somos jóvenes los telómeros miden entre 8.000 y 15.000 pares de bases, las unidades con que se mide el ADN.
Con la edad ese número va cayendo. En la piel los telómeros se acortan aproximadamente 9 pares de bases por año en la epidermis, la capa exterior, y 11 pares de bases por año en la dermis, la capa más profunda donde viven los fibroblastos que producen colágeno.
Eso significa que en 30 años de vida adulta los telómeros de tu dermis pierden alrededor de 330 unidades solo por el paso del tiempo.
El problema no es ese ritmo normal. El problema es cuando factores externos lo aceleran.
Los telómeros no miden cuántos años tienes, miden cómo has vivido.
Dos mujeres de 45 años pueden tener longitudes teloméricas completamente distintas. Una puede tener telómeros equivalentes a los de una mujer de 38 años. La otra puede tenerlos equivalentes a los de una mujer de 55 años.
La diferencia no está en el tiempo que pasó, está en lo que ese tiempo tuvo adentro.
Un estudio publicado en la Proceedings of the National Academy of Sciences, uno de los más citados en este campo, encontró que las mujeres con niveles altos de estrés sostenido tenían telómeros equivalentes a una década adicional de envejecimiento celular comparadas con mujeres de la misma edad pero con bajo estrés.
Una década. No en el espejo — en las células.
El estrés crónico es uno de los más documentados. El cortisol elevado de manera sostenida aumenta el estrés oxidativo y el ADN telomérico es especialmente vulnerable al daño oxidativo porque tiene una secuencia química particular que lo hace más reactivo. El estrés no solo se siente, se deposita en el ADN.
El mal sueño también tiene evidencia sólida. Un estudio publicado en 2025 confirmó que el trabajo nocturno prolongado se asocia con acortamiento telomérico y lo más fascinante es que ese acortamiento fue parcialmente reversible al recuperar los ritmos normales de sueño. El cuerpo puede corregir parte del daño cuando le das las condiciones para hacerlo.

La inflamación crónica activa un ambiente que presiona a las células a dividirse más y cada división acorta los telómeros. El inflammaging que hemos visto en artículos anteriores no solo daña desde afuera, presiona el reloj celular desde adentro.
El estrés oxidativo daña directamente el ADN telomérico. Y como vimos en los artículos sobre mitocondrias — cuando las mitocondrias no funcionan bien producen más radicales libres que aceleran ese daño.
Todo está conectado. Siempre.
El NAD+ activa unas enzimas llamadas sirtuinas en particular SIRT1 y SIRT6. Y SIRT6 tiene una función específica y documentada en el mantenimiento y protección de los telómeros.
Cuando el NAD+ cae con la edad, y ya vimos que cae, SIRT6 no puede hacer su trabajo con la misma eficiencia. Los telómeros quedan más expuestos al daño. Y el acortamiento se acelera.
Restaurar el NAD+ no solo apoya la energía mitocondrial, también protege la integridad del ADN telomérico. El sistema funciona en conjunto.
Si leíste nuestro artículo sobre células zombi, recordarás que cuando los telómeros llegan a un largo crítico la célula entra en senescencia.
No muere, pero deja de dividirse y empieza a secretar moléculas inflamatorias que dañan el entorno. Y ese ambiente inflamatorio a su vez acelera el acortamiento telomérico en las células vecinas.
Es un círculo y entenderlo es lo que permite interrumpirlo.
Un meta-análisis que reunió 20 estudios con casi 3.000 participantes encontró que la combinación de ejercicio físico y alimentación antioxidante puede aumentar la longitud telomérica de manera independiente a la edad o condición inicial.
El sueño de calidad y los ritmos circadianos regulares protegen los telómeros directamente. Dormir mal no es solo cansancio, es presión sobre el reloj celular.

La alimentación rica en antioxidantes reduce el daño oxidativo al ADN telomérico. La dieta mediterránea se asocia consistentemente con telómeros más largos en múltiples estudios.
Y el manejo del estrés no como concepto vago sino como práctica real, tiene evidencia directa en la preservación telomérica.
El WOW Shower Gel tiene como función principal eliminar las células muertas acumuladas en el estrato córneo, la capa más superficial de la piel. Importante aclarar: estas células muertas no son lo mismo que las células senescentes, son células que completaron su ciclo normal y se acumulan en la superficie opacando la piel. Al eliminarlas con su complejo de 5 AHA de origen natural, el gel mejora la textura, unifica el tono y prepara la piel para recibir mejor lo que viene después. Una piel renovada en su superficie responde mejor en profundidad.
El WOW Oil trabaja en sincronía con el ciclo nocturno de reparación, el momento en que el cuerpo dedica más energía a regenerarse. El masaje ascendente con ácido ricinoleico activa la microcirculación y el drenaje linfático, mejorando el transporte de oxígeno y nutrientes hacia los tejidos dérmicos. Una dermis bien oxigenada produce menos estrés oxidativo, uno de los principales factores que aceleran el acortamiento telomérico.
THE EXOSO+NAD actúa directamente en los dos mecanismos celulares más relacionados con la protección telomérica. RejuveNAD™ estimula la producción endógena de NAD+, activando las sirtuinas SIRT1 y SIRT6 que protegen y reparan el ADN telomérico. Sin NAD+ suficiente esas enzimas no pueden hacer su trabajo. PhytoCellTec™ Exosomes reactiva la comunicación entre fibroblastos y células madre mesenquimales, las células dérmicas más vulnerables cuando los telómeros se acortan y la senescencia avanza.
No alarga los telómeros. Apoya los mecanismos que los protegen y reduce los factores que los deterioran más rápido.
La pregunta que me cambió todo no fue cuántos años tengo.
Fue cómo los he vivido.
Con mucho cariño, Andrea 🤍
Conoce el Protocolo CellCare en thewowbenefits.cl

Fuentes:
Liu, Z. et al. (2025). Telomeres in skin aging. Biogerontology 26, 83. DOI: 10.1007/s10522-025-10228-9
Epel, E.S. et al. (2004). Accelerated telomere shortening in response to life stress. PNAS 101(49), 17312–17315.
Ferrari, L. et al. (2025). Impact of night shift work on telomere length. Journal of Occupational Medicine and Toxicology 20:31.
Lehodey, A. et al. (2026). Telomere dynamics influenced by sleep and circadian rhythms. Alzheimer’s Research & Therapy 18:10.
Arsenis, N.C. et al. (2022). Effect of a lifestyle intervention on telomere length. Ageing Research Reviews.